张文东医生的科普号
- 专科知识介绍 肺栓塞诊断流程
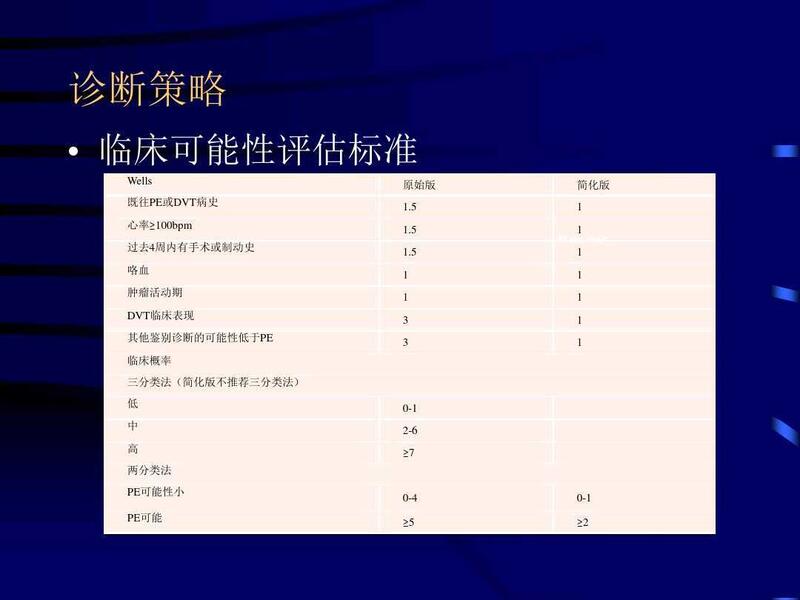
ACP临床指南委员会的最佳实践建议--肺栓塞指南 低风险患者:临床医生应该应用肺栓塞排除标准(PERC)八项;如果患者满足所有8个诊断标准,则检查造成的不利风险就会比较高,因此没必要进行检查。通过避
 张文东 主任医师 六安市中医院 呼吸内科2079人已读
张文东 主任医师 六安市中医院 呼吸内科2079人已读 - 专科知识介绍 发热伴血小板减少综合征诊疗方案
发热伴血小板减少综合征诊疗方案 为指导各地及时、有效地开展发热伴血小板减少综合征的诊断和救治工作,依据现有的临床和实验室资料,制定本方案。随着临床经验积累以及对本病认识的深入,将进一步修订完善。 一、临床表现 潜伏期尚不十分明确,可能为1周~2周。急性起病,主要临床表现为发热,体温多在38℃以上,重者持续高热,可达40℃以上,部分病例热程可长达10天以上。伴乏力、明显纳差、恶心、呕吐等,部分病例有头痛、肌肉酸痛、腹泻等。查体常有颈部及腹股沟等浅表淋巴结肿大伴压痛、上腹部压痛及相对缓脉。 少数病例病情危重,出现意识障碍、皮肤瘀斑、消化道出血、肺出血等,可因休克、呼吸衰竭、弥漫性血管内凝血(DIC)等多脏器功能衰竭死亡。 绝大多数患者预后良好,既往有基础疾病、老年患者、出现精神神经症状、出血倾向明显、低钠血症等提示病重,预后较差。 二、实验室检查 (一) 血常规检查。外周血白细胞计数减少,多为1.0-3.0×109/L,重症可降至1.0×109/L以下,嗜中性粒细胞比例、淋巴细胞比例多正常; 血小板降低,多为30-60×109/L,重症者可低于30×109/L。 (二) 尿常规检查。 半数以上病例出现蛋白尿(+~+++),少数病例出现尿潜血或血尿。 (三) 生化检查。 可出现不同程度LDH、CK及AST、ALT等升高,尤以AST、CK-MB升高为主,常有低钠血症,个别病例BUN升高。 (四)病原学检查。 1.血清新型布尼亚病毒核酸检测。 2.血清中分离新型布尼亚病毒。 (五) 血清学检查。 1.新型布尼亚病毒IgM抗体(尚在研究中)。 2.新型布尼亚病毒IgG抗体。 三、诊断与鉴别诊断 (一)诊断标准。 依据流行病学史(流行季节在丘陵、林区、山地等地工作、生活或旅游史等或发病前2周内有被蜱叮咬史)、临床表现和实验室检测结果进行诊断。 1. 疑似病例:具有上述流行病学史、发热等临床表现且外周血血小板和白细胞降低者。 2. 确诊病例:疑似病例具备下列之一者:(1)病例标本新型布尼亚病毒核酸检测阳性;(2)病例标本检测新型布尼亚病毒IgG抗体阳转或恢复期滴度较急性期4倍以上增高者;(3)病例标本分离到新型布尼亚病毒。 (二)鉴别诊断。 应当与人粒细胞无形体病等立克次体病、肾综合征出血热、登革热、败血症、伤寒、血小板减少性紫癜等疾病相鉴别。 四、治疗 本病尚无特异性治疗手段,主要为对症支持治疗。 患者应当卧床休息,流食或半流食,多饮水。密切监测生命体征及尿量等。 不能进食或病情较重的患者,应当及时补充热量,保证水、电解质和酸碱平衡,尤其注意对低钠血症患者补充。高热者物理降温,必要时使用药物退热。有明显出血或血小板明显降低(如低于30×109/L)者,可输血浆、血小板。中性粒细胞严重低下患者(低于1×109/L),建议使用粒细胞集落刺激因子。 体外实验结果提示利巴韦林对该病毒有抑制作用,临床上可以试用。继发细菌、真菌感染者,应当选敏感抗生素治疗。同时注意基础疾病的治疗。目前尚无证据证明糖皮质激素的治疗效果,应当慎重使用。 五、出院标准 体温正常、症状消失、临床实验室检查指标基本正常或明显改善后,可出院。 六、隔离及防护 一般情况下无需对病人实施隔离。医护人员和看护人接触病人时应当采取通用防护(Universal precaution )措施。对病人的血液、分泌物、排泄物及被其污染的环境和物品,可采取高温、高压、含氯消毒剂等方式进行消毒处理。在抢救或护理危重病人时,尤其是病人有咯血、呕血等出血现象时,医务人员及陪护人员应当加强个人防护,避免与病人血液直接接触。
张文东 主任医师 六安市中医院 呼吸内科1989人已读 - 专科进展 2023CSCO诊疗指南:IA、IB期非小细胞肺癌的治疗
注释:(1)肺癌外科手术标准:肺癌手术应做到完全性切除。1)完全性切除①切缘阴性,包括支气管、动脉、静脉、支气管周围、肿瘤附近组织。②淋巴结至少6组,其中肺内3组;纵膈3组(必须包括7区)。③切除的最高淋巴结镜下阴性。④淋巴结无结外侵犯。2)不完全性切除①切缘肿瘤残留。②胸腔积液或心包积液癌细胞阳性。③淋巴结结外侵犯。④淋巴结阳性但不能切除。3)不确定切除:切缘镜下阴性,但出现下列情况之一者①淋巴结清扫未达要求。②切除的最高纵膈淋巴结阳性。③支气管切缘为原位癌。④胸腔冲洗液细胞学阳性。(2)先进放疗技术包括4D-CT和PET/CT定位系统、VMAT(容积旋转调强放射治疗技术)、IGRT(影像引导放射治疗)、呼吸运动控制、质子治疗等。(3)辅助化疗IA期非小细胞肺癌不建议辅助化疗,IB期非小细胞肺癌(包括有高危因素的肺癌),由于缺乏高级别证据的支持,常规不推荐辅助化疗。(4)不完全切除患者二次手术±化疗(2A类)或术后三维适形放疗±化疗[IB期(2A类),IA期(2B类)]。(5)肺部病灶切除范围日本II期临床研究JCOG0804/WJOG4507L显示,肿瘤实性成分比值(CTR)≤0.25且病灶目≤3个、长径≤2cm的周围型N0肺癌,足够切缘的亚肺叶切除可提供很好的局部控制和RFS,期待该研究更详细的数据。JCOG0802是一项多中心、开放、随机对照、非劣效III期临床研究,旨在比较肺段切除和肺叶切除在IA期[肿瘤实性成分比值(CTR)>0.5;肿瘤长径≤2cm)]NSCLC中的疗效与安全性。研究结果显示:肺段切除组和肺叶切除组相比,5年OS率更高,分别为94.3%和91.1%(HR=0.663,P<0.001)。5年无复发生存时间,两组相当(肺段切除组:88%vs.肺叶切除组:87.9%,HR=0.998,P=0.9889)。CALGB140503比较了在T1aN0(肿瘤直径≤2cm)NSCLC中肺叶切除和亚肺叶切除(解剖性肺段切除或楔形切除)的疗效。研究结果显示:亚肺叶切除组的无疾病生存期非劣效于肺叶切除组(HR=1.01;95%CI0.72-1.26)。基于上述两项研究结果,本指南新增“胸腔镜下解剖学肺段切除或楔形切除[限T1N0(≤2cm)及肺野外1/3病灶]”并作为II级推荐。
 张文东 主任医师 六安市中医院 呼吸内科11人已读
张文东 主任医师 六安市中医院 呼吸内科11人已读 - 专科进展 2023CSCO诊疗指南:IIA、IIB期非小细胞肺癌的治疗
注释:(1)可选辅助化疗方案包括:长春瑞滨/紫杉醇/多西他赛/培美曲塞(非鳞癌)/吉西他滨+顺铂/卡铂。(2)对于IIA期患者,完全性切除后,可考虑给予辅助化疗。(3)对于EGFR突变阳性患者,NMPA已批准奥希替尼或埃克替尼用于术后辅助治疗。(4)IMpower010研究结果显示,对于II-IIIA期适宜手术患者,根治性手术及含铂双药化疗后,阿替利珠单抗对比最佳支持治疗显著延长了PD-L1≥1%患者的无病生存期(未达到vs.35.3个月,HR=0.66,P=0.004),基于此,NMPA已批准阿替利珠单抗用于II-IIIA期PD-L1≥1%且接受根治性手术及含铂双药化疗后的辅助治疗,本指南将“根治性手术后,阿替利珠单抗辅助治疗(限PD-L1≥1%)”从II级推荐上升至I级推荐。(5)KEYNOTE-091/PEARLS研究结果显示:对于IB(T2a≥4cm)-IIIA期适宜手术患者,根治性手术及含铂双药化疗后,帕博利珠单抗对比安慰剂显著延长了患者的无病生存期(53.6个月vs.40.2个月,HR=0.76,P=0.0014),基于此,美国FDA已批准帕博利珠单抗用于IB(T2a≥4cm)-IIIA期NSCLC切除和铂类化疗后的辅助治疗,本指南新增“根治性手术后,帕博利珠单抗辅助治疗”并作为II级推荐。(6)CheckMate816研究结果显示,对于IB-IIIA期适宜手术患者,纳武利尤单抗联合化疗与单独化疗相比,显著延长中位无事件生存期(31.6个月vs.20.8个月,HR=0.63,P=0.005)。基于此,NMPA已批准纳武利尤单抗联合含铂双药化疗用于肿瘤直径≥4cm或淋巴结阳性的可切除NSCLC新辅助治疗,本指南新增“化疗联合纳武利尤单抗新辅助治疗II-IIIA期NSCLC患者”并作为I级推荐。在临床实践中,建议严格按照药物适应症推荐治疗,不宜将同类药物进行简单替换。(7)卡瑞丽珠、信迪利、替雷利珠单抗联合治疗(联合化疗或抗血管治疗)等多个II期新辅助研究在II-IIIA期NSCLC患者中展现出良好效果。近期,特瑞普利单抗联合含铂双药作为新辅助治疗的III期研究Neotorch公布达到主要研究终点(无事件生存期)。一项研究卡瑞丽珠单抗联合阿帕替尼作为IIA-IIIB期(仅T3N2M0)新辅助治疗的II期研究显示,MPR率为57%,pCR率为23%,显示治疗前景。(8)不完全切除患者,行二次手术+含铂双药化疗或术后放疗+含铂双药方案化疗。(9)对于不适宜手术患者,可考虑采用同步放化疗,化疗方案一般参考III期患者的方案。
 张文东 主任医师 六安市中医院 呼吸内科7人已读
张文东 主任医师 六安市中医院 呼吸内科7人已读 - 专科进展 2023CSCO诊疗指南:可手术IIIA或IIIB(T3N2M0)期非小细胞肺癌的治疗
注释:IIIA期NSCLC是高度异质性的一组疾病。根据IASLC/UICC第8版分期,IIIA期包括:T3N1、T4N0-1和T1-2bN2。在治疗前完整分期检查的基础上,根据治疗前初评是否可行完全性切除,可将IIIA期NSCLC分为3组:①可完全性手术切除,即R0切除;②可能完全性手术切除;③无法完全性切除。根据术后病理N分期,可将患者分为pN0-1和pN2两个亚组。对于T3N2M0,在IASLC/UICC第8版分期中划为IIIB期,对于非侵袭性T3,可考虑新辅助化疗+手术±辅助化疗±术后放疗,或同步放化疗;对于侵袭性T3,建议同步放化疗。(1)临床判断可完全性手术切除的IIIA期NSCLC包括T3N1、部分T4N1(如肿瘤直接侵犯胸壁、主支气管或纵膈)伴或不伴单站纵膈淋巴结转移的病变。对于该组患者,推荐首先进行手术切除,术后辅助含铂双药方案化疗;若术后病理N分期为N0-1,不需进行术后放疗;若病理分期为N2,是否需进行术后放疗尚存争议,详见病理N2期NSCLC的术后放疗。另一基本策略为根治性同步放化疗(详见IIIB期NSCLC的治疗)。可选策略为新辅助治疗后再行根治性切除(详见IIIA期NSCLC的新辅助治疗)。目前,NMPA已批准阿替利珠单抗用于II-IIIA期PD-L1TC≥1%且接受根治性手术及含铂双药化疗后的辅助治疗,本指南将“根治性手术后,阿替利珠单抗辅助治疗(限PD-L1TC≥1%)”从II级推荐上升至I级推荐。美国FDA已批准帕博利珠单抗用于IB(T2a≥4cm)-IIIA期NSCLC切除和铂类化疗后的辅助治疗,本指南新增“根治性手术后,帕博利珠单抗辅助治疗”并作为II级推荐。另外,NMPA已批准纳武利尤单抗联合含铂双药化疗用于肿瘤≥4cm或淋巴结阳性的可切除NSCLC新辅助治疗,本指南新增“化疗联合纳武利尤单抗新辅助治疗II-IIIA期NSCLC患者”并作为I级推荐。(2)局部侵犯胸壁但无纵膈淋巴结转移(T3N1)的肺上沟瘤目前推荐的治疗为新辅助同步放化疗后进行完全性手术切除,2年生存率为50%-70%,5年生存率为70%。对于不能直接进行R0切除的IIIA期NSCLC,基本策略为根治性同步放化疗(详见IIIB期NSCLC的治疗)。可选策略为新辅助治疗后(详见IIIA期NSCLC的新辅助治疗),再评估,决定给予完全性切除或是继续放化疗至根治剂量。目前尚无高类别证据显示新辅助化疗后联合手术能够优于根治性放化疗,也无证据表明新辅助放化疗+手术的三联疗法能够优于化疗+手术或根治性放化疗的二联疗法。对于同一肺叶内多个病灶的T3病变和同侧肺不同肺叶内多个病灶的T4病变,推荐治疗为肺叶切除或全肺切除术后辅助化疗。对于术后病理分期为N0-1的患者,不推荐术后放疗;对于术后N2患者,除辅助化疗外(2A类),是否进行术后放疗尚存争议(详见病理N2期NSCLC的术后放疗)。(3)无法进行完全性切除的病变如肿瘤局部侵犯很广、预计新辅助治疗后仍无法达到R0切除、多站纵膈淋巴结转移,首选治疗方式为根治性放化疗(1类),目前尚无证据支持后续巩固化疗,详见IIIB期NSCLC的治疗。同步化疗方案主要包括顺铂+依托泊苷;卡铂+紫杉醇或顺铂/卡铂+培美曲塞。同步化疗首推方案为顺铂+依托泊苷;放疗推荐剂量为60-70Gy,目前尚无证据表明提高局部放疗剂量能够改善疗效。PACIFIC研究是一项针对不可手术切除的局部晚期NSCLC根治性同步放化疗后,予以PD-L1抑制剂度伐利尤单抗巩固治疗对比安慰剂的III期随机对照研究。结果显示同步放化疗后度伐利尤单抗巩固治疗组的PFS显著优于安慰剂组(中位PFS,16.8个月vs.5.6个月,HR=0.52,P<0.001)。且度伐利尤单抗巩固治疗组的疾病缓解率、疾病缓解维持时间、发生远处转移或死亡的时间均显著优于对照组。基于PACIFIC研究的结果,美国FDA批准其用于局部晚期NSCLC同步放化疗后的巩固治疗。在不良反应方面,度伐利尤单抗组3或4度不良反应发生率,因不良反应治疗中断率要高于对照组。NMPA批准度伐利尤单抗在国内上市,用于同步放化疗后未进展的不可切除的III期NSCLC患者的巩固治疗。PACIFIC5年更新随访数据证实度伐利尤单抗巩固治疗组的5年OS率(42.9%),显著高于对照组(33.4%)。此外,国内一项评估真实世界PACIFIC治疗模式的meta分析也得到类似结论。基于上述研究结果,对于符合条件的患者,亦鼓励参加同步放化疗后PD-1/PD-L1单抗巩固治疗相关临床研究。(4)EGFR突变阳性患者术后辅助治疗EGFR-TKI辅助治疗进行了广泛的探索。BR.19以及PADIANT研究均探索了TKI在EGFR突变非选择人群中的术后辅助治疗价值,均以失败告终。EVIDENCE研究对比了埃克替尼与标准辅助化疗在II-IIIA期伴EGFR突变NSCLC完全切除术后辅助治疗的疗效与安全性,埃克替尼显著延长中位DFS(47.0个月vs.22.1个月,HR=0.36,P<0.0001)。ADAURA研究是探索奥希替尼作为辅助治疗的III期临床研究,结果显示,在II-IIIA期患者中,与安慰剂组相比,奥希替尼显著延长了II-IIIA期患者的中位DFS(65.8个月vs.21.9个月,HR=0.23,P<0.001)。值得注意的是,ADAURA研究纳入了IB期患者,但由于其属于亚组分析,且研究采用的分期为第7版分期,故本指南暂不将奥希替尼加入IB期NSCLC患者术后辅助的I级推荐。对于EGFR突变阳性切接受TKI辅助治疗的IIIA期NSCLC,术后辅助放疗的作用和时机尚不明确。ADJUVANT研究是吉非替尼对比长春瑞滨+顺铂方案的前瞻性随机、对照III期临床试验。与化疗相比,吉非替尼显著延长了中位DFS(18.0个月vs.28.7个月,HR=0.60,P=0.0054),但未显著延长中位OS。另一项厄洛替尼对比含铂双药化疗作为完全切除术后、伴有EGFR突变的IIIA期NSCLC患者的辅助治疗的疗效与安全性的II期临床研究(EVAN研究)。结果显示,与化疗相比,厄洛替尼显著延长中位DFS(42.4个月vs.21.0个月,HR=0.268,P<0.001)及中位OS(61.1个月vs.51.1个月,HR=0.318,P=0.0015)。但来自日本的IMPACT研究结果显示,EGFR突变阳性患者术后接受吉非替尼辅助与标准含铂双药治疗相比,无论DFS或OS均未得到统计学阳性结果,提示EGFR突变肺癌患者术后辅助靶向治疗尚存在争议。(5)IIIA期NSCLC的新辅助治疗对于部分IIIA/N2期NSCLC,已有多项探讨各种新辅助治疗联合手术模式对比传统根治性放化疗的随机对照研究。迄今为止,前期发表的联合治疗模式包括诱导化疗后手术对比放疗(EORTC08941:IIIA/N2新辅助化疗3周期后随机接受手术vs.根治性放疗)、诱导放化疗后手术对比根治性放疗(INT0139:pN2患者,新辅助同步放化疗后接受手术vs.根治性同步放化疗,并都辅以2个周期巩固化疗)、新辅助化疗后手术对比新辅助序贯放化疗后手术(SAKK:IIIA/N2新辅助化疗3个周期后根治性手术vs.新辅助诱导化疗序贯放疗44Gy/22次后根治性手术)、新辅助化疗+序贯同步放化疗后根治性手术对比新辅助化疗后序贯根治性放化疗(ESPATUE:IIIA/N2期和部分选择性IIIB,3个周期的PC方案新辅助化疗后同步放化疗,45Gy/1.5Gy,每日2次x3周,同步1个周期顺铂+长春瑞滨,可切除病变接受推量至根治性放化疗vs.根治性手术)、新辅助靶向治疗后手术对比新辅助含铂双药化疗后手术(CTONG1103:IIIA/N2新辅助厄洛替尼治疗42天后接受手术vs.吉西他滨+顺铂新辅助治疗2个周期后手术)以及免疫检查点抑制剂(PD-1单抗或PD-L1单抗)为基础的新辅助治疗后手术等。在化疗药物时代,无论是新辅助化疗+手术还是新辅助放化疗+手术较同步放化疗均未显示出生存获益。因此,根治性同步放化疗仍然是IIIA/N2期NSCLC的标准治疗。CTONG1103研究是一项来自中国17个中心的开放标签、随机对照II期研究,针对EGFR敏感突变IIIA期(N2)NSCLC患者,比较厄洛替尼对比吉西他滨+顺铂(GC)方案作为新辅助治疗的疗效和安全性,共72例患者接受治疗,32例(91.4%)完成了两个周期的新辅助GC化疗。研究未达到主要终点,厄洛替尼和GC新辅助治疗的ORR分别为54.1%和34.3%(P=0.092)。后续公布的OS数据发现两组中位OS差异无统计学意义。目前多项免疫检查点抑制剂(PD-1单抗或PD-L1单抗)为基础的方案作为早中期NSCLC新辅助治疗的研究已经完成入组并公布了初步结果。CheckMate816研究结果显示,对于IB-IIIA期适宜手术患者,纳武利尤单抗联合化疗与单独化疗相比,显著延长中位五事件生存期(31.6个月vs.20.8个月,HR=0.63,P=0.005)。基于此,NMPA已批准纳武利尤单抗联合含铂双药化疗用于肿瘤≥4cm或淋巴结阳性的可切除NSCLC新辅助治疗。卡瑞丽珠、信迪利、替雷利珠单抗联合治疗等多个II期新辅助研究在II-IIIA期NSCLC患者中展现出良好效果。一项研究卡瑞丽珠单抗联合阿帕替尼作为IIA-IIIB期(仅T3N2M0)新辅助治疗的II期研究显示,MPR率为57%,pCR率为23%。Neotorch研究是一项随机、双盲、多中心III期研究,评估特瑞普利联合含铂双药化疗在可切除的IIA-IIIB期NSCLC患者中的疗效,近期公布达到主要研究终点(无事件生存期)。这些研究结果显示以PD-1单抗或PD-L1单抗为基础的新辅助治疗具有较好的应用前景,但尚需总生存数据的支持。综上所述,根治性同步放化疗作为主要治疗模式的地位仍未动摇。对于可手术患者,新辅助治疗联合手术可作为治疗选择之一,但新辅助治疗模式(单纯化疗、序贯化放疗、同步放化疗、化疗后同步放化疗、靶向治疗以及免疫检查点抑制剂为基础的治疗)仍待进一步研究,鼓励患者参加相关的临床试验。(6)病理N2期NSCLC的术后放疗略
 张文东 主任医师 六安市中医院 呼吸内科11人已读
张文东 主任医师 六安市中医院 呼吸内科11人已读 - 专科进展 2023CSCO诊疗指南:不可手术IIIA、IIIB、IIIC期非小细胞肺癌的治疗
注释:第8版IASLC/UICC肺癌分期指南已广泛应用,因此本指南中添加了关于IIIC期的相关治疗推荐,同时对推荐表格下方的备注部分进行了相应的修改。本指南中,有根治性治疗可能(意愿)且PS评分良好的患者,如放疗设备、放疗计划的剂量参数符合剂量学要求,则推荐同步放化疗。对于放射治疗,至少应予以患者基于CT定位的三维适形放疗(3D-CRT)。推荐采用常规剂量分割方式,靶区剂量(60-66)Gy/(30-33)次/(6-7)周。RTOG0617研究表明,进一步增加放疗总剂量至74Gy并不能提高疗效。非计划放疗中断导致的放疗总治疗时间延长,不利于放疗效果的提高。超分割或加速超分割放疗的相关临床研究表明,缩短总治疗时间能显著改善长期生存。但这类放疗技术引起放疗并发症的可能性更高,其临床应用性受到一定限制,目前只能在一些选择性患者中开展。关于纵膈淋巴结预防放疗,同步放化疗或序贯化放疗,均推荐基于PET/CT检查和IMRT现代放射治疗技术进行累及野的选择性淋巴结区域照射。PACIFIC研究是一项针对不可手术切除的局部晚期NSCLC根治性同步放化疗后,予以PD-L1抑制剂度伐利尤单抗巩固治疗对比安慰剂的III期随机对照研究。结果显示同步放化疗后度伐利尤单抗巩固治疗组的PFS显著优于安慰剂组(中位PFS,16.8个月vs.5.6个月,P<0.001),且度伐利尤单抗巩固治疗组的疾病缓解率、疾病缓解维持时间、发生远处转移或死亡的时间均显著优于对照组。在不良反应方面,度伐利尤单抗组3或4度不良反应发生率、因不良反应导致治疗中断率要高于对照组。部分因各种原因不能耐受同步放化疗的患者,可以采用序贯化疗-根治性放疗模式,研究证实该治疗策略较单纯放疗可改善生存获益。对于序贯化放疗或同步放化疗未进展患者,GEMSTONE-301研究显示,舒格利单抗巩固治疗对比安慰剂显著延长了无进展生存期(中位10.5个月vs.6.2个月,HR=0.65;同步放化疗组:15.7个月vs.8.3个月,HR=0.71;序贯放化疗组:8.1个月vs.4.1个月,HR=0.57)。NMPA已批准舒格利单抗作为同步或序贯放化疗后的功能治疗用于不可手术局部晚期NSCLC,故本指南将“舒格利单抗作为同步或序贯放化疗后的巩固治疗”从III级推荐上升至I级推荐。有证据表明,诱导化疗后行同步放化疗不优于直接同步放化疗,同样,III期临床研究没有显示出放化疗后加巩固化疗对患者有长期生存获益。对于PS=2,难以耐受同步放化疗的患者,单纯放疗或序贯放疗+化疗为推荐的治疗模式,序贯放疗+化疗能够进一步提高患者生存获益。单纯根治性放疗可用于因PS=2或严重合并症而不适合放化综合治疗策略的患者,通过提高患者治疗耐受性而获得潜在的生存获益。对于难以耐受或不愿意接受放疗的患者,可予以化疗,化疗方案参照IV期驱动基因阴性患者NSCLC中的化疗方案推荐,根据患者的不同病理类型,选择适宜的化疗方案。不可切除患者经诱导治疗后可否手术目前存在较多争议,尚无一个明确的推荐指南。提示对这类患者在治疗开始时应该进行有效的个体化多学科会诊,其重要性可能远胜于一个设计好的精确治疗路径或协议。新进研究(ESPATUE)显示,部分不可切除的III期患者经诱导化疗或放化疗后获益,T、N分期明显降期,转变为可手术切除。手术切除和根治性放化疗比较,尽管术后PFS和OS没有增加,但亚组分析显示选择性患者(T3N2,T4N0-1)(AJCC第7版分期指南)有明显的长期生存获益,尤以IIIB(T4N0-1)显著。总之,目前没有1类证据推荐常规新辅助放疗或放化疗加手术的治疗模式。目前除临床研究外,新辅助放疗没有适应症。新辅助治疗后可切除的III期患者,如切缘(+),患者临床条件许可,可术后同步放化疗,如切缘(-),可行浒关术后化疗-放疗,术后放疗可提高患者的局部控制率。非随机研究显示,一些先进放疗技术如4D-CT或PET/CT模拟技术,结合IGRT、VMAT、TOMO和质子放疗对比常规3D-CRT和IMRT放疗,可减少放疗毒性,改善疗效。但实施这类新技术应参考ACR-ASTRO放疗实践指南,进行临床研究。目前尚无同步放疗+TKI治疗不可切除IIIA期、IIIB期、IIIC期非小细胞肺癌生存获益的临床证据。
 张文东 主任医师 六安市中医院 呼吸内科8人已读
张文东 主任医师 六安市中医院 呼吸内科8人已读 - 专科进展 2023CSCO诊疗指南:IV期BRAF V600等少见突变非小细胞肺癌的治疗
注释:近年来,国内外针对少见驱动基因靶点的临床研究产生重大突破,除EGFR/ALK/ROS1突变外,BRAFV600/NTRK/MET14外显子/RET/KRASG12C均已获得美国FDA或NMPA批准上市,此外,HER-2突变NSCLC的靶向治疗也迎来曙光。针对BRAFV600突变的晚期NSCLC,一项达拉非尼联合曲美替尼一线治疗BRAFV600E突变晚期NSCLC的II期临床研究(NCT01336634)结果显示ORR为64%,中位PFS为10.9个月,中位DoR为10.4个月。美国FDA已批准达拉非尼联合曲美替尼用于BRAFV600突变转移性NSCLC的一线治疗。若联合治疗不耐受,可单用达拉非尼。目前,NMPA已批准达拉非尼联合曲美替尼治疗BRAFV600突变晚期NSCLC并纳入医保,因此本指南将其上调为I级推荐。针对NTRK突变的晚期NSCLC,STARTRK-2、STARTRK-1和ALKA-372-001三项临床研究的汇总结果显示,BICK评估的恩曲替尼治疗后NTRK融合实体瘤患者的ORR为57.0%,中位PFS为11.2个月,DoR为10.4个月,颅内客观反应率为50.0%。2019年美国FDA已批准恩曲替尼用于NTRK融合基因阳性实体瘤的治疗。一项发表在《新英格兰医学杂志》上总共纳入55例NTRK融合实体瘤患者的研究显示拉罗替尼治疗ORR为75%,在1年时研究者评估,71%的患者应答持续,55%的患者保持无进展。因此美国FDA批准拉罗替尼用于无已知获得性耐药突变的NTRK融合肿瘤患者。目前,NMPA已批准恩曲替尼和拉罗替尼治疗NTRK融合晚期NSCLC,因此本指南将其上调为I级推荐。针对MET14外显子跳跃突变的晚期NSCLC,赛沃替尼作为国内自主研发的MET抑制剂,II期临床研究数据显示,独立评审委员会(IRC)评估的ORR为49.2%,DCR为93.4%,DoR达6个月。亚组分析显示,赛沃替尼治疗其他类型NSCLC患者的DCR达到95.1%,中位PFS达到9.7个月。基于此,NMPA已批准赛沃替尼用于治疗MET外显子14跳跃突变的后线治疗并纳入医保。故本指南将其上调为I级推荐。II期临床研究GEOMETRYmono-1研究针对卡马替尼治疗MET外显子14跳突的NSCLC患者,结果显示卡马替尼对初治患者的ORR为68%,DoR超过12个月的患者比例为47%;经治患者的ORR为41%,DoR超过12个月的患者比例为32%.此外另一项VISION研究揭示了特泊替尼治疗含MET外显子14跳突的晚期NSCLC的有效性和安全性。根据液体活检或组织活检确定是否检测到MET外显子14跳跃突变,结果显示特泊替尼在血液+组织联合活检组的有效率为46%,mDoR达11.1个月,液体活检组66例,有效率为48%,组织活检组60例,有效率为50%。基于此,美国FDA已批准卡马替尼和特泊替尼用于一线和后线治疗局部晚期或转移性MET外显子14跳突的NSCLC患者,但国内尚未批准上市,因此本指南仅将两者作为III级推荐。谷美替尼是国产的新型MET抑制剂,单臂II期GLORY研究评估了谷美替尼治疗携带METex14跳突的局部晚期或转移性NSCLC的有效性和安全性。结果显示:总体ORR为60.9%;在初治患者中,ORR为66.7%;在经治患者中,ORR为51.9%。总体人群PFS为7.6个月。针对RET融合的晚期NSCLC,ARROW研究结果显示,RET抑制剂普拉替尼(BLU-667)在接受或未接受治疗的RET融合阳性NSCLC患者中均显示出临床获益,经治患者ORR为62%,PFS为16.5个月;初治患者ORR为79%,PFS为13.0个月。基于ARROW研究阳性结果,普拉替尼于2021年被NMPA批准上市,用于既往接受过含铂化疗的RET融合基因阳性晚期NSCLC患者,因RET融合基因为罕见突变,开展随机对照研究难,经专家组投票后决议,本次指南将其上调为I级推荐。鉴于2022年10月NMPA已受理普拉替尼治疗晚期RET融合阳性NSCLC一线治疗申请,且美国FDA已批准普拉替尼一线治疗RET融合阳性晚期NSCLC。经专家组投票,本次指南新增“普拉替尼一线治疗RET融合阳性晚期NSCLC”并作为II级推荐。LIBRETTO-001研究探索了赛普替尼(LOXO-292)在RET融合患者中的疗效和安全性,结果显示ORR为64%,DoR达17.5个月,DoR超过6个月的患者比例为81%。NMPA已批准赛普替尼用于RET融合阳性晚期NSCLC,因此本指南将其上调为I级推荐。针对KRASG12C突变的晚期NSCLC,CodeBreak100II期临床研究结果显示,Sotorasib(AMG510)治疗KRAS突变NSCLC的ORR为37.1%,DCR为80.6%,中位PFS为6.8个月。此外,Adagasib(MRTX849)在KRASG12C突变的晚期NSCLC中也显示出了良好的抗肿瘤活性,KRYSTAL01临床研究结果显示,Adagasib(MRTX849)的ORR为43%,DCR为80.0%,中位PFS为6.5个月,中位OS为12.6个月。2022年FDA已批准Adagasib上市,用于携带KRASG12C突变的NSCLC患者的后线治疗,但国内尚未上市,因此本指南将其作为III级推荐。针对HER2突变的晚期NSCLC,吡咯替尼作为一种广泛ErbB受体络氨酸激酶抑制剂,显示出良好的疗效。目前关于吡咯替尼治疗HER2突变型铂类化疗后晚期肺腺癌的II期临床研究(NCT02834936)结果显示,经IRC评估的ORR为30.0%,DoR为6.9个月,中位PFS为6.9个月,中位OS为14.4个月,且安全性良好。NMPA已批准吡咯替尼联合卡培他滨应用于HER2阳性晚期乳腺癌,但尚未批准NSCLC适应症。因此本指南将其作为HER2突变NSCLC后线治疗的III级推荐。此外,德喜曲妥珠单抗(DS-8201a)在HER2突变的晚期NSCLC也显示出良好的抗肿瘤活性,客观缓解率、中位无进展生存期、中位总生存期分别为55%、8.2个月、17.8个月,目前FDA已批准德喜曲妥珠单抗用于后线治疗HER2突变晚期NSCLC,且中国于2023年2月获批其乳腺癌适应症,经专家组投票,上调其为III级推荐。
 张文东 主任医师 六安市中医院 呼吸内科10人已读
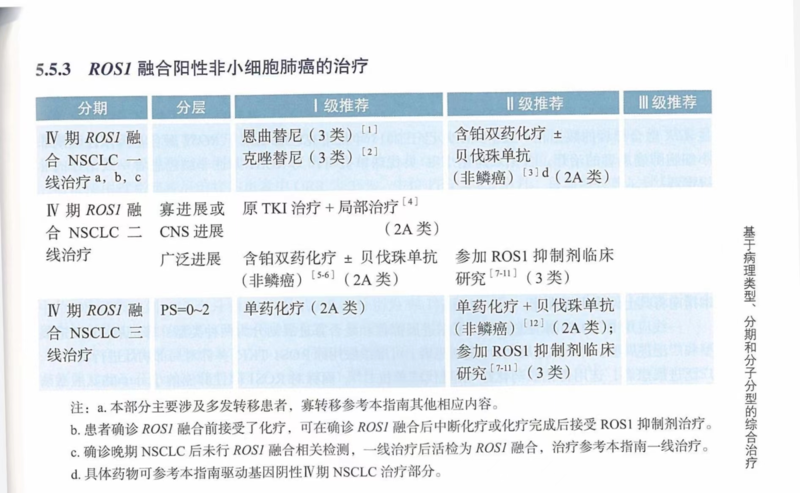
张文东 主任医师 六安市中医院 呼吸内科10人已读 - 专科进展 2023CSCO诊疗指南:IV期ROS1融合阳性非小细胞肺癌的治疗
注释:目前ROS1融合基因阳性IV期NSCLC一线推荐应用克唑替尼,主要基于OO1201,克唑替尼治疗ROS1融合基因阳性晚期NSCLC的PFS为15.9个月,ORR为71.7%,安全数据与既往ALK融合患者的数据一致,NMPA已于2017年批准克唑替尼用于ROS1融合基因阳性晚期NSCLC患者的治疗。含铂双药化疗±贝伐珠单抗可作为ROS1阳性非鳞癌患者一线治疗的II级推荐。恩曲替尼在ROS1阳性患者的治疗中也取得了突破性进展。STARTRK-2、STARTRK-1和ALKA-372-001三项临床研究的汇总结果显示,在53例局部晚期或转移性ROS1阳性NSCLC患者中,BICR评估的恩曲替尼治疗后ORR为77.0%,中位PFS为19.0个月,中位DoR为24.6个月;颅内客观反应率55.0%。目前,NMPA已批准恩曲替尼用于ROS1融合基因阳性晚期NSCLC的治疗,因此本指南将其上调为I级推荐。一线应用ROS1抑制剂进展后,根据进展部位和是否寡进展划分为两种类型:寡进展/CNS进展型和广泛进展型。对于寡进展/CNS进展患者,可继续服用原ROS1-TKI,并针对局部病灶进行治疗。广泛进展患者,选用含铂双药化疗±贝伐珠单抗。而针对ROS1阳性肺癌的小分子络氨酸激酶抑制剂还包括塞瑞替尼、他雷替尼(AB-106)、洛拉替尼、Repotrectinib等,在I期或II期临床研究中显示出了令人鼓舞的疗效。他雷替尼(AB-106)为新型ROS1/NTRK靶向药,I期研究结果显示AB-106治疗未经克唑替尼治疗的患者(9例)的ORR为66.7%,中位PFS为24.9个月,而治疗克唑替尼耐药患者(9例)的ORR为33.3%,中位PFS为7.6个月。2021年ASCO会议公布了II期临床研究结果显示,共有15例未经过克唑替尼治疗和5例接受过克唑替尼治疗的ROS1融合阳性非小细胞肺癌患者入组治疗。在未经过克唑替尼治疗的患者中(n=15),ORR为93%,DCR为93%;在曾接受过克唑替尼治疗的患者(n=5)中,ORR为60%,DCR为100%。洛拉替尼为第三代ALK/ROS1靶向药,洛拉替尼治疗ROS1阳性NSCLC的单臂I/II期临床结果显示,纳入了ROS1阳性69例患者中,21例TKI初治患者ORR为62%,中位PFS为21.0个月。40例之前仅使用过克唑替尼治疗的患者中ORR为35%,中位PFS为8.5个月。目前洛拉替尼针对ROS1阳性肺癌的研究正在国内展开。TPX0005(Repotrectinib)是新一代ROS1/NTRK1-3靶向药,2020年WCLC公布了TRIDENT-1的I/II期研究结果,I/II期共入组22例患者,经IRC确认的ORR为91%,II期部分纳入15例患者,经经IRC确认的ORR为93%。TQ-B3101是一种新型的ROS1抑制剂,在2022年ELCC公布的一项单臂、II期研究显示,IRC评估的ORR为78.4%,中位DoR为20.3个月,中位OS尚未达到,12个月和24个月的OS率分别为98.1%和88.1%。对于ROS1融合NSCLC靶向及含铂双药均失败的患者,可选用单药化疗+贝伐珠单抗或参与上述新药的临床研究。关于免疫治疗,虽然ROS1与ALK同源性较高,但PD-1/PD-L1治疗的疗效与ALK阳性患者存在差异,ImmunoTarget研究入组了7例ROS1阳性NSCLC患者,缓解率为17%,目前关于ROS1免疫治疗的数据较少,需要更多的研究验证,本指南尚未推荐相关药物。目前ROS1阳性患者克唑替尼进展后治疗方案的选择并无太多数据,但鉴于ROS1与ALK的同源性及克唑替尼同样适用于ALK阳性患者,本指南推荐采用与ALK阳性患者靶向治疗进展后类似的处理模式。对于克唑替尼及化疗进展后的患者,推荐参加其他ROS1抑制剂的临床试验。
 张文东 主任医师 六安市中医院 呼吸内科11人已读
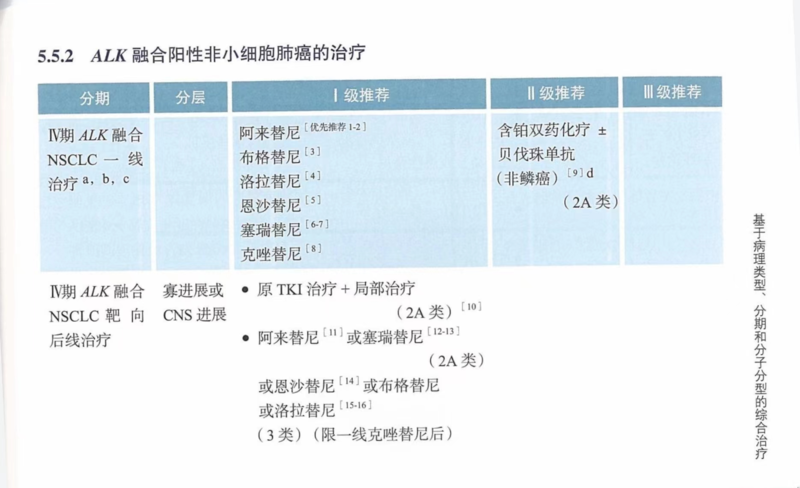
张文东 主任医师 六安市中医院 呼吸内科11人已读 - 专科进展 2023CSCO诊疗指南:IV期ALK融合阳性非小细胞肺癌的治疗
注释:ALK融合阳性晚期NSCLC目前国内获批的药物有克唑替尼、阿来替尼、塞瑞替尼、恩沙替尼、布格替尼和洛拉替尼。在亚洲人群中进行的阿来替尼与克唑替尼头对头比较的III期临床研究,ALESIA研究的结果与ALEX研究一致,阿来替尼组PFS显著延长(中位PFS,未达到vs.11.1个月,HR=0.22,P<0.001);颅内客观缓解率阿来替尼组达94.1%,显著优于克唑替尼组的28.6%,降低脑转移发生风险86%(HR=0.14,P<0.0001)。就该研究结果,我国NMPA于2018年批准阿来替尼用于ALK阳性的局部晚期或转移性NSCLC,包括一线及克唑替尼治疗进展后的二线用药。ALESIA研究更新的阿来替尼一线治疗中位PFS为41.6个月。III期临床研究ASCEND-4研究证实了塞瑞替尼在未经治疗的ALK阳性NSCLC患者中的疗效。研究显示,塞瑞替尼组中位PFS为16.6个月,化疗组中位PFS为8.1个月。由于塞瑞替尼耐受性不佳,另一项多中心随机临床研究ASCEND-8研究比较了塞瑞替尼450mg/d随餐服用及750mg/d空腹服用的疗效及安全性,450mg随餐服用同750mg空腹服用患者的血药浓度相似,但胃肠毒性显著降低。450mg组患者的依从性更好,其15个月无进展生存期较750mg空腹给药组更高(66.4%vs.41%)。PROFILE1014研究证实一线克唑替尼疗效优于含铂双药化疗,PFS显著延长(中位,10.9个月vs.7.0个月,P<0.001),ORR显著提高(74%vs.45%,P<0.001)。含铂双药化疗±贝伐珠单抗可作为ALK阳性非鳞癌患者一线治疗的II级推荐。eXalt3研究结果表明,在ITT人群中,与克唑替尼相比,恩沙替尼显著改善了PFS(25.8个月vs.12.7个月),可使疾病进展或死亡风险降低49%(HR=0.51,P<0.001)。ALTA-IL研究结果显示,在亚洲和非亚洲人群中,与克唑替尼相比,布格替尼均显著改善PFS,使用布格替尼的亚洲人群疾病进展风险下降59%(中位PFS未达到vs.11.1个月,HR=0.41,P=0.0261),基线伴脑转移患者的颅内PFS在亚洲人群(HR=0.15,P=0.0037)较克唑替尼也均有显著改善。CROWN研究结果表明,与克唑替尼相比,第三代ALK抑制剂洛拉替尼显著改善了PFS(中位,未达到vs.9.3个月,HR=0.28),1年PFS率为78%vs.39%,可使疾病进展或死亡风险降低72%(HR=0.28,P<0.001)。基于上述研究结果,NMPA已批准恩沙替尼、布格替尼和洛拉替尼一线治疗ALK阳性NSCLC患者,因此本指南更新上述ALK-TKIs一线治疗均予以I级推荐。一线应用ALK抑制剂进展后,根据进展部位和是否寡进展划分为两种类型:寡进展/CNS进展型和广泛进展型。对于寡进展/CNS进展患者,可继续服用原ALK-TKI,并针对局部病灶进行治疗。若一线应用克唑替尼治疗,可更换为阿来替尼、塞瑞替尼、恩沙替尼、布格替尼、洛拉替尼。因布格替尼和洛拉替尼获NMPA批准全线适应症,本指南上调其推荐级别为I级。若一线使用一代ALK抑制剂克唑替尼出现广泛进展,推荐使用二代ALK抑制剂。阿来替尼治疗克唑替尼失败后的ALK阳性晚期NSCLC的全球II期研究NP28673中,IRCORR为50%,中位PFS为8.9个月,在可评估的有CNS病灶的患者,ORR为57%,中位DoR为11.2个月。欧洲和亚洲人群的III期随机对照研究ALUR显示,在克唑替尼及至少一次化疗治疗失败的患者中,与培美曲塞或多西他赛相比。阿来替尼显著降低疾病进展风险达85%(HR=0.15,P<0.001),中位PFS分别为阿来替尼组9.6个月,化疗组1.4个月。塞瑞替尼ASCEND-1研究入组了部分经克唑替尼治疗失败的患者,其ORR和PFS分别为56%和7.0个月。塞瑞替尼治疗克唑替尼耐药后的ALK阳性NSCLC的ASCEND-2研究的结果ORR为38.6%,IRC评估的中位PFS为7.2个月。恩沙替尼治疗ALK阳性晚期NSCLC克唑替尼耐药单臂多中心II期临床研究结果显示,ORR达52%,颅内ORR70%,中位PFS达9.6个月。布格替尼的II期临床研究(NCT02094573)将克唑替尼耐药后患者分为A、B组:A组,布格替尼90mg,1次/天;B组,连续7天布格替尼90mg后增至180mg,1次/天。研究者评估的ORR,A组达45%,B组达54%;独立评审委员会评估的中位PFS,A组9.2个月,B组15.6个月;基线伴脑转移的颅内ORR为A组42%,B组67%。基于此研究,2017年FDA批准布格替尼用于ALK阳性晚期NSCLC克唑替尼耐药后的治疗。洛拉替尼全球II期临床研究(NCT01970865)结果显示,后线治疗既往使用克唑替尼±化疗的患者,ORR达72.9%,颅内ORR达87.5%,中位PFS为11.1个月;后线治疗既往使用≥1种二代ALK-TKI±克唑替尼的患者,ORR为39.6%,颅内ORR高达56.1%,中位PFS为6.6个月。因布格替尼和洛拉替尼已获NMPA批准全线适应症,本指南上调其推荐级别为I级。一项II期临床研究评估了ALK/ROS1-TKI伊鲁阿克(WX0593)在ALK阳性NSCLC一线克唑替尼耐药后的疗效。在146例患者中,IRC评估的ORR为67.8%,中位PFS为14.4个月,18个月的OS率为81.9%。一项I期研究评估了TQ-B3139(CT-711)的疗效与安全性。在TKI经治患者中,ORR为37.5%,中位PFS为5.4个月。目前,NMPA已批准阿来替尼、洛拉替尼、恩沙替尼及塞瑞替尼全线治疗ALK阳性晚期NSCLC适应症,因此可作为一线TKI耐药后的治疗选择。ALK抑制剂靶向治疗均告失败的患者,推荐选用含铂双药化疗±贝伐珠单抗。此外,ALK抑制剂耐药后,可根据患者有无症状、转移部位及数目来综合选择后续治疗方案。研究发现,克唑替尼耐药后30%-45%的耐药机制依赖于ALK通路,包括ALK激酶域二次突变(包括C1156Y、L1196M等)和ALK拷贝数增加,而二代ALK-TKI(阿来替尼和塞瑞替尼)更容易发生Solvent-front区域突变(50%-70%),针对不同ALK-TKI耐药突变,治疗策略不同。例如洛拉替尼可以克服G1202R耐药,塞瑞替尼、布格替尼、洛拉替尼均对V1180L和L1196M突变有效。但目前该方面的数据有限,仅有临床前数据和小样本病例报道,因此本次指南更新暂未推荐按照耐药机制选择后续治疗。ALK阳性NSCLC在TKI及含铂双药均进展后的治疗,PS评分为0-2分的患者,可以考虑单药化疗。ALTER0303研究入组了7例ALK融合基因阳性的患者,安罗替尼治疗也显示一定的获益,但建议在安罗替尼治疗前,应接受相应的标准靶向药物治疗后进展、且至少接受过2种系统化疗后出现进展或复发。另外,抗PD-1/PD-L1免疫单药治疗在ALK融合阳性患者中疗效有限。
 张文东 主任医师 六安市中医院 呼吸内科13人已读
张文东 主任医师 六安市中医院 呼吸内科13人已读 - 专科进展 2023CSCO诊疗指南:IV期EGFR突变非小细胞肺癌的治疗
注释:EGFR突变阳性晚期NSCLC患者一线治疗的多个随机对照研究显示,吉非替尼、厄洛替尼、埃克替尼、阿法替尼对比化疗均可改善患者的PFS,且3度及以上不良反应显著低于化疗。LUX-Lung7、ARCHER1050研究、FLAURA、AENEAS和FURLONG研究分别显示阿法替尼、达可替尼、奥希替尼、阿美替尼和伏美替尼疗效优于一代TKI,奠定了第一代EGFR-TKI吉非替尼、厄洛替尼、埃克替尼,第二代TKI阿法替尼、达可替尼以及第三代TKI奥希替尼、阿美替尼和伏美替尼在EGFR突变晚期NSCLC一线治疗的地位。NMPA已批准伏美替尼一线治疗适应症并纳入医保,因此本指南新增“伏美替尼用于IV期EGFR敏感突变NSCLC一线治疗”并作为I级推荐。二代EGFR-TKI较一代EGFR-TKI具有更优的疗效,但不良反应也显著增加,ARCHER1050研究中接受达可替尼治疗的患者,近2/3因不良反应需要剂量调整。FLAURA研究显示三代EGFR-TKI奥希替尼较一代EGFR-TKI显著延长中位PFS(18.9个月vs.10.2个月,P<0.001)和中位OS(38.6个月vs.31.8个月,P=0.0462),但亚裔亚组分析OS无明显差异。AENEAS研究显示阿美替尼一线治疗对比吉非替尼显著延长中位PFS(19.3个月vs.9.9个月,HR=0.46,P<0.0001)。FURLONG研究显示富媒体你一线治疗对比吉非替尼可显著延长中位PFS(20.8个月vs.11.1个月,HR=0.44,P<0.0001)。在贝福替尼作为一线治疗晚期EGFR突变NSCLC患者的III期临床研究中,对比埃克替尼组,贝福替尼组显示出更优的中位PFS(22.1个月vs.13.8个月,HR=0.49,P<0.0001)。目前,贝福替尼尚未批准上市。联合治疗模式,包括EGFR-TKI联合化疗或抗血管生成治疗,也为EGFR突变阳性患者一线治疗的选择。II期随机对照JMIT研究中,吉非替尼联合培美曲塞组PFS优于吉非替尼单药(中位PFS,15.8个月vs.10.9个月,P=0.029)。III期研究NEJ009以及印度开展的III期研究探讨了TKI联合含铂双药化疗,结果均显示吉非替尼联合培美曲塞+卡铂组较吉非替尼单药组显著延长PFS,并且OS也显著延长。NEJ026研究是一项在日本开展的随机、开放、多中心III期临床试验。结果显示:贝伐珠单抗联合厄洛替尼相比厄洛替尼单药一线治疗晚期EGFR敏感突变型非鳞NSCLC,虽可显著延长患者的PFS(16.9个月vs.13.3个月,HR=0.605),但两组中位OS差异无统计学意义(50.7个月vs.46.2个月,HR=1.007)。III期随机对照研究CTONG1509也证实贝伐珠单抗与厄洛替尼联合方案相比厄洛替尼单药显著延长中位PFS(18.0个月vs.11.3个月,P<0.001)。也有研究提示贝伐珠单抗联合厄洛替尼对伴有脑转移的EGFR突变患者有更优的疗效。由于靶向治疗耐药后治疗手段增多,虽有研究显示部分EGFR-TKI耐药的患者继续接受靶向治疗仍有短暂获益,EGFR-TKI耐药后缓慢进展的患者也应该尽快接受后续的抗肿瘤治疗。根据进展部位和是否寡进展划分为两种类型:寡进展型和广泛进展型。对于寡进展/CNS进展患者,多个回顾性分析显示继续原EGFR-TKI治疗联合局部治疗可获益。同时,由于三代EGFR-TKI奥希替尼、阿美替尼、伏美替尼对于中枢神经转移病灶有效率高,寡进展/CNS进展的患者亦推荐行驱动基因突变检测,辅助指导后续治疗。EGFR-TKI耐药后再活检耐药机制分析显示T790M突变为50%左右。对比奥希替尼和铂类双药化疗治疗TKI耐药后T790M阳性的NSCLC的随机III期AURA3临床研究显示,奥希替尼显著延长PFS(中位PFS,10.1个月vs.4.4个月,P<0.001)。AURA17研究进一步在亚裔人群中评估了奥希替尼治疗TKI耐药后T790M阳性患者的疗效,BIRC评估的ORR为62%,中位PFS为9.7个月,中位OS为23.2个月。阿美替尼治疗一代EGFR-TKI进展的T790M阳性的NSCLC的多中心、单臂II期临床研究显示ORR为68.4%,且耐受性好。第三代EGFR-TKI伏美替尼治疗EGFRT790M突变晚期NSCLC受试者的IIB期临床研究(NCT03452592),结果显示ORR为74%,DCR为94%,PFS为9.6个月。此外,多个国产三代EGFR-TKI,包括奥瑞替尼、瑞泽替尼、贝福替尼、ASK1200在TKI耐药后T790M阳性NSCLC治疗中也显示出良好的疗效,ORR在60%左右,中位PFS12个月左右,目前CDE已受理上市申请。EGFR外显子20插入突变占所有EGFR突变的4%-12%。莫博赛替尼(Mobocertinib,TAK-788)治疗含铂化疗期间或之后进展的EGFRex20ins突变NSCLC患者的I/II期临床研究结果显示:中位OS为24.0个月,中位PFS为7.3个月,ORR为28%且安全可控。CHRYSALIS研究结果显示EGFR/MET双特异性抗体Amivantamab用于治疗EGFRex20ins局部晚期或转移性NSCLC,ORR为40%,PFS为8.3个月,OS为22.8个月。基于此,2021年美国FDA批准Amivantamab上市。目前,NMPA已批准莫博赛替尼用于含铂化疗进展的EGFRex20insNSCLC治疗。在中国II期单臂注册WU-KONG6临床研究中,舒沃替尼治疗EGFRex20ins突变ORR在总体人群达到59.8%,目前该药物已获得CDE突破性治疗药物品种认定。基于LUX-LUNG2、3、6合并分析阿法替尼治疗少见突变的研究,阿法替尼还被美国FDA批准用于18-21外显子少见位点突变(Leu861Gln、Gly719Ser、Gly719Ala、Gly719Cys、Ser768lle)患者的治疗。此外,联合小分子抗血管抑制剂阿帕替尼一线治疗EGFR突变NSCLC的ACTIVE研究也显示出阳性结果,共313例患者入组研究,阿帕替尼与吉非替尼联合组中位PFS(IRCC)为13.7个月(HR=0.71,95%CI0.54-0.95,P=0.0189),较单纯吉非替尼治疗组延长了3.5个月,但NMPA尚未批准。若EGFR靶向耐药后不存在T790M突变,化疗目前仍为经典的治疗选择。IMPRESS研究在一线吉非替尼耐药后的患者中对比了化疗和化疗联合吉非替尼的疗效,联合用药的患者的PFS并没有延长,吉非替尼联合化疗组OS反而低于单纯化疗组(中位OS,13.4个月vs.19.5个月,HR=1.44,P=0.016)。一项特瑞普利单抗联合化疗用于EGFR-TKI治疗失败的EGFR突变阳性T790M阴性晚期NSCLC患者的II期临床研究结果显示ORR达50%,DCR达87.5%,中位DoR为7.0个月,整体人群PFS达7.0个月。多个III期临床研究正在探讨化疗联合免疫治疗在EGFR-TKI耐药患者中的地位。对于免疫联合治疗,IMpower150研究入组了EGFR及ALK阳性的患者,结果提示阿替利珠单抗+化疗+贝伐珠单抗的疗效相比阿替利珠单抗+化疗或化疗+贝伐珠单抗都有显著提高,客观缓解率达71%,中位PFS达10.2个月,中位OS超过25个月;既往接受过EGFR-TKI靶向治疗的患者仍能从四药联合治疗中获益。欧盟2019年批准了这一四药联合方案,包括作为EGFR-TKI耐药后患者的后线治疗,但这一方案在EGFR突变患者中的应用前景,期待IMpower151临床研究结果的公布。III期ORIENT-31临床研究中期分析显示,信迪利单抗+贝伐珠单抗+化疗对比安慰剂+化疗,显著延长了无进展生存期(6.9个月vs.4.3个月,HR=0.464,P<0.0001)。本指南将其作为携带EGFR敏感突变晚期NSCLC的TKI治疗后广泛进展的III级推荐方案。ORIENT-31在2022年ESMO年会上公布了信迪利单抗+化疗对比安慰剂+化疗的分析数据,结果显示:与化疗相比,信迪利单抗+化疗显著延长了中位PFS(5.5个月vs.4.3个月,HR=0.723,P=0.0181)。但在另一项评估在EGFR-TKI耐药后标准含铂化疗基础上联合免疫治疗的随机III期试验CheckMate722研究中,相比于单纯化疗,化疗联合纳武利尤单抗并未显著改善患者的PFS(5.6个月vs.5.4个月,HR=0.75,P=0.053)。近期公布的KEYNOTE-789研究结果也未能证实化疗联合帕博利珠单抗可为患者带来PFS和OS获益。因此,基于目前临床研究数据,EGFR-YKI耐药后,化疗联合免疫治疗的疗效还存在一定争议,化疗+免疫治疗是否成为TKI耐药后的治疗选择尚需进一步探索。其他EGFR-TKI耐药的原因还包括EGFR扩增、MET扩增、HER-2扩增、PIK3CA突变、BRAF突变以及SCLC转换等。目前针对BRAF、HER-2、MET等多个靶点都有相应的临床试验在进行,EGFR-TKI耐药后可进行再活检明确耐药原因以指导下一步治疗。安罗替尼的III期临床研究(ATLER0303)结果显示,对比安慰剂,安罗替尼能够显著延长患者中位OS和PFS,OS延长3.3个月(中位OS,9.6个月vs.6.3个月,P=0.0018),死亡风险下降32%;PFS延长4.0个月(中位PFS,5.4个月vs.1.4个月,P<0.0001)。2018年5月,安罗替尼获NMPA批准用于既往至少接受过2种系统化疗后出现或复发的局部晚期或转移性NSCLC患者的治疗,对于存在EGFR突变或ALK融合阳性的患者,在开始安罗替尼治疗前应接受相应的标准靶向药物治疗后进展,且至少接受过2种系统化疗后出现进展或复发。
 张文东 主任医师 六安市中医院 呼吸内科10人已读
张文东 主任医师 六安市中医院 呼吸内科10人已读





